Menjelaskan nama unsur dan nama rurnus kimia sederhana
A. UNSUR
Sampai saat ini dikenal lebih dari 100 macam unsur, kita belajar mengenal dari unsur-unsur yang sederhana. Lambang unsur diusulkan oleh orang yang berasal dari Negara Swedia Pada tahun (1779-1 848) yang bernama Jons Jakob Berzelius.
Usulan dari jons Jakob Berzelius:
• Lambang unsur diambil dari huruf depannya dari nama latin unsur tersebut. misal oksigen lambangnya O.
• Jika nama depan sudah dipakai suatu unsur maka diikuti huruf kedua misel calsium lambangnya Ca.
CONTOH LAMBANG DARI BEBRAPA UNSUR
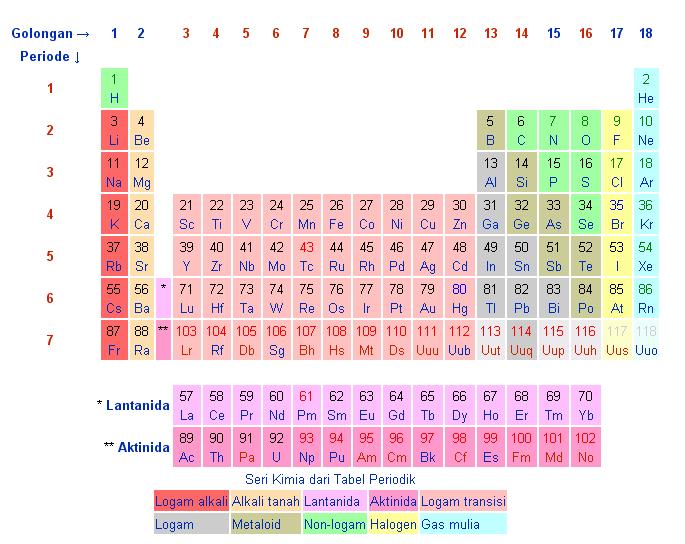

Membandingkan sifat unsur, senyawa dan campuran
A. KLASIFIKASI MATERI
Berdasarkan konsep kimia materi dapat diklasifikasikan:
Materi terdiri dari:
a. Zat tunggal terdiri dari
i. Unsur
ii. Senyawa
b. Campuran terdiri dari:
i. Campuran homogen
ii. Campuran heterogen
B. UNSUR
Unsur adalah zat yang paling sederhana, unsur tidak dapat diuraikan melalui reaksi kimia menjadi zat lain yang lebih sederhana. Sampai saat ini telah dikenal lebih dari 100 macam unsur, sembilan puluh dua diantaranya merupakan unsur alam sedang sisanya merupakan unsur buatan.
Contoh unsur alam diantaranya : alumunium, emas, besi carbon, belerang, oksigen, nitrogen, kalium; pospor, tembaga, seng, kalsium, natrium. Sedangkan contoh unsur buatan adalah Curium, Ameresium, Nobellum dan Einstenium.
Disebut unsur buatan karena adanya dibuat manusia sedangkan unsur alam artinya bahan dasarnya secara alamiah sudah tersedia, contoh besi, mineral yang mengandung besi secara aiamiah sudah tersedia.
Unsur dapat dibedakan menjadi 3 kelompok yaitu unsur logam, unsur non logam dan metalloid. Sifat unsur logam diantaranya mengkilap, penghantar listrik yang baik, mempunyai titik didih dan titik leleh yang relatif tinggi. Unsur non logam mempunyai sifat isolator, tidak mengkilap mempunyai titik didih dan titik leleh yang relatif rendah. Sedangkan metalloid adalah unsur yang mempunyai sifat logam dan non logam misalnya yang sudah terkenal adalah Silikon. Mengenal lambang unsur sudah diberikan contohnya di awal.
C. SENYAWA
Senyawa adalah zat hasil reaksi atau persenyawaan dari dua unsur atau lebih. Melalui reaksi kimia senyawa dapat diuraikan menjadi unsur-unsur pembentuknya kembali. Contoh senyawa sederhana yang paling banyak dikenal masyarakat misalnya etanol terkenal dengan nama alcohol, garam dapur atau natrium clorida gula pasir atau sukrosa.
Sifat penting senyawa adalah mempunyai susunan tetap. Artinya perbandingan massa unsur-unsur pembentuknya dalam senyawa adalah tetap (Joseph Proust). Contoh perbandingan massa unsur-unsur pembentuk air adalah tetap yaitu massa hydrogen : mässa oksigen 1 : 8.
BEBERAPA PERBANDINGAN UNSUR DALAM PEM8ENTUKAN SENYAWA


Carbon dioksida rumusnya CO2 Perbandingan massa unsur pembentuknya C: 0 = 3:8
Carbon monooksida rumusnya CO Perbandingan massa unsur pembentuknya C: 0 = 3: 4
Glukosa rumusnya C5H1206 Perbandingan massa unsur pembentuknya C: H : 0 6: 1: 8
Air rumusnya HO Perbandingan massa unsur pembentuknya H : 0 = 1: 8
Belerang tn oksida rumusnya SO3 Perbandingan massa unsur pembentuknya S : 0 2 : 3
Contoh:
Untuk membuat carbon di oksida jika tersedia carbon = 60 gram , maka akan memerlukan oksigen sebanyak 160 gram ( lihat perbandingan C : 0 = 3 : 8 ). Sehingga massa carbon di oksida yang dihasilkan sebãnyak 220 gram Disamping berlaku Hukum Proust maka pada pembentukan senyawa juga berlaku Hukum Kekekalan massa ( Lavoisier ) yaitu massa zat sebelum reaksi sama dengan massa zat sesudah reaksi.
Tidak ada komentar:
Posting Komentar